Resumen:
Los compuestos activos de Cannabis sativa se estudian ampliamente por sus efectos terapéuticos, más allá de la conocida actividad psicotrópica. C. Sativa, se utiliza para tratar diferentes indicaciones médicas, como esclerosis múltiple, espasticidad, epilepsia, colitis ulcerosa y dolor. Simultáneamente, la investigación básica es descubrir nuevos constituyentes de compuestos derivados del Cannabis y sus receptores capaces de la neuroprotección y la modulación de la actividad neuronal. La función de los diversos fitoquímicos en diferentes procesos terapéuticos no se comprende completamente, pero su papel significativo está comenzando a emerger y ser apreciado. En esta revisión, consideraremos la relación estructura-actividad (SAR) de los compuestos cannabinoides capaces de unirse a los receptores de cannabinoides y actuar como agentes terapéuticos en las enfermedades neuronales, por ejemplo, la enfermedad de Parkinson.
Palabras clave:
Cannabis sativa ; relación estructura-actividad; fitocannabinoides; endocannabinoides; receptores cannabinoides; enfermedades neuronales; enfermedad de Parkinson
1. Introducción
La planta de marihuana, Cannabis sativa L., produce cientos de metabolitos secundarios. C. sativa produce un grupo diverso de policetidos de resorcinil isoprenilados comúnmente llamados fitocannabinoides. Las vías de construcción de los fitocannabinoides «similares a Lego», a través de las transformaciones no enzimáticas inducidas por el calor, la luz y el oxígeno atmosférico, producen diferentes cadenas laterales de resorcinilo o variaciones en el grado de oligomerización del extremo de isoprenilo, creando alquil y un Quimotipos de β-aralquilos . Estos incluyen alrededor de 110 fitocannabinoides característicos, los más estudiados de los cuales son dronabinol (Δ 9-tetrahidrocannabinol, THC) y cannabidiol (CBD). Esta planta ha sido conocida durante miles de años por su efecto en el cuerpo humano . El efecto psicoactivo de C. sativa , producido por solo uno de sus cientos de constituyentes supuestamente llevó a su cultivo hace más de 6000 años . Se cree que la antigua C. sativa se utiliza para diversos fines sociales y rituales, e incluso en aplicaciones paliativas y medicinales .
Hoy en día, C. sativa se usa medicinalmente para tratar varias indicaciones médicas. El inventario integrado de estos compuestos y sus puntos finales macromoleculares biológicos resaltan las oportunidades que ofrecen los fitocannabinoides para acceder a efectos deseables similares a los medicamentos, más allá de la asociada con el objetivo narcótico CB1 . El principal compuesto activo con efectos psicotrópicos producidos por el THC de la planta, es probablemente el compuesto que alivia el dolor neuropático crónico, náuseas, dolores de cabeza y fatiga. Sin embargo, otros compuestos activos de C. sativa.puede explicar sus actividades médicas adicionales en diversos tejidos y partes del cuerpo, como epilepsia, náuseas inducidas por quimioterapia , anorexia , espasticidad de esclerosis múltiple , fibromialgia y reumatoide artritis , glaucoma presiones intraoculares y disnea asociada al asma .
Además de los fitocannabinoides, C. sativa produce más de 400 fitoquímicos, incluidos terpenoides y terpenos, flavonoides e hidrocarburos . Aunque recientemente se ha publicado un inventario completo y unificado de fitocannabinoides , aún queda mucho por aprender acerca de la actividad de los diferentes fitoquímicos, sus modos de acción en el cuerpo humano y sus relaciones estructura-actividad (SAR). En esta revisión, nos centraremos en el SAR de compuestos naturales y sintéticos de C. sativa que pueden unirse a los receptores de cannabinoides acoplados a proteína G y pueden ser beneficiosos en el tratamiento de enfermedades neuronales, por ejemplo, la enfermedad de Parkinson.
1.1. Receptores de cannabinoides y endocannabinoides
Hasta la fecha se conocen tres tipos de receptores de cannabinoides acoplados a proteínas G (GPCR): en primer lugar, CB1, clonado en 1990 y CB2, clonado en 1993 fueron ampliamente reconocidos y estudiados como objetivos efectivos de los cannabinoides. Mucho más tarde, se sugirió un tercer cannabinoide acoplado a proteína G, el receptor 55, como CB3 . El CB3 comparte varios cannabinoides con los dos GPCR reconocidos previamente, pero con una homología baja con los receptores de cannabinoides clásicos . Su fisiopatología es todavía vaga y sus funciones en el sistema nervioso central aún no se comprenden, aunque se demostró que el CB3 se expresa en varias áreas del cerebro .
La evidencia también sugiere que los cannabinoides se unen y actúan a través de los receptores nucleares activados por el proliferador de peroxisomas (PPAR, por sus siglas en inglés), con tres subtipos α, β (δ) y γ) . Los receptores cannabinoides se distribuyen en el cuerpo humano, principalmente en el sistema nervioso central, pero también en otros tejidos periféricos, como el bazo, el tracto reproductivo, urinario y gastrointestinal, las glándulas endocrinas, las arterias y el corazón . Se investigó la existencia de subtipos adicionales de receptores de cannabinoides en el sistema endocannabinoide . Modulación del sistema endocannabinoide utilizando C. sativa.tiene efectos terapéuticos prometedores en el tratamiento de diversos trastornos, como enfermedades neurodegenerativas , epilepsia , déficits cognitivos y otros. Sin embargo, producir fármacos derivados de cannabinoides para tratar estos trastornos mediante la regeneración o modificación del sistema endocannabinoide es un gran desafío y aún no se ha logrado .
Los endocannabinoides se producen en el cuerpo cuando es necesario, bajo estrés o en respuesta a la actividad sináptica . Los endocannabinoides más estudiados son la anandamida ortostérica (AEA) y 2-AG . Se considera que son dominantes y son agonistas de los receptores CB1 y CB2, con mayor afinidad por la unión a CB1 . Todavía se necesita una caracterización farmacológica adicional para comprender a fondo las funciones fisiológicas de los endocannabinoides y sus modos de acción . Sin embargo, la manipulación farmacológica de los niveles de endocannabinoides puede proporcionar nuevas oportunidades para regular el sistema endocannabinoide y tratar los trastornos relacionados .
1.2. Fitocannabinoides
Originalmente, el término «cannabinoide» se refería a una clase homogénea de monoterpenoides típica de C. sativaL. Más recientemente, el término «cannabinoides» se ha extendido a todos aquellos compuestos que muestran una afinidad por el GPCR conocido como receptores de cannabinoides, CB1 y CB2, independientemente de su esqueleto monoterpenoide (se sabe muy poco acerca de GPR55, también llamado CB3, en este respeto). Los análogos producidos de forma endógena que muestran afinidad por CB1 y CB2 se conocen como endocannabinoides. Para diferenciarse de esta última clase de compuestos, se ha introducido el término fitocannabinoides para enfatizar el origen botánico de estos cannabinoides. Entre los cannabinoides derivados de plantas conocidos, los más abundantes son los tetrahidrocannabinoles (THCs), los cannabidioles (CBD) y los cannabinoles (CBN), seguidos de los cannabigeroles (CBG), los cannabicromenos (CBC) y los cannabinodioles (CBNDs, Figura 1 ) .
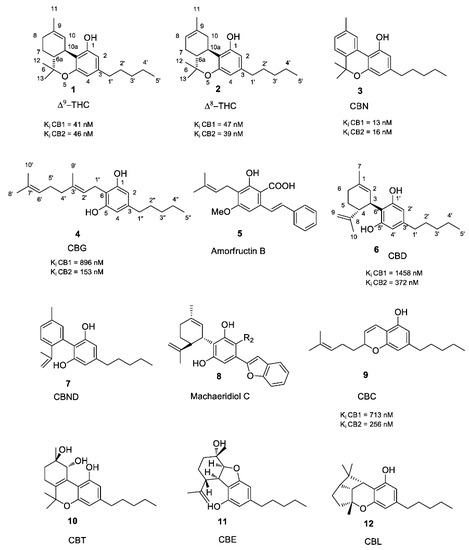
Figura 1. Estructura de los fitocannabinoides narcóticos Δ 8 -THC, 9 -THC, CBN con alta afinidad por los receptores CB1 y CB2 y de fitocannabinoides no narcóticos CBG y CBD. Se reportan sistemas de numeración y afinidades vinculantes.
Los fitocannabinoides clásicos son compuestos terpenoides tricíclicos que contienen un resto de benzopirano soluble en lípidos y solventes orgánicos no polares. Los compuestos fenólicos son solubles, ya que las sales de fenolato se forman en condiciones básicas. En la planta, la forma carboxilada de los cannabinoides es más abundante, denominada «ácido» e indicada como THCA, CBDA, CBGA y similares. Los compuestos psicoactivos son la forma descarboxilada de las variedades, es decir, THC, etc. Existen algunas variaciones en la longitud de la cadena lateral C-3, siendo el pentilo el más común, pero los derivados de n- propilo también son bien conocidos. Los análogos n- propilados con su cadena más corta se nombran usando el sufijo «varin» y se indican como THCV, CBDV y similares .
Como se mencionó anteriormente, los fitocannabinoides se clasifican, en base a la cadena lateral de resorcinol, en dos clases principales: (a) alquilo y (b) β-aralquilo . Como la cadena lateral β-aralquilo se deriva de un iniciador aromático, su residuo reemplaza al grupo alquilo de los compuestos originales. Las subclases de estas dos clases principales se identifican además en función de la naturaleza de la cadena lateral y de la presencia de puentes O con un núcleo de resorcinol .
1.2.1. Compuestos de Cannabigerol (CBG)
Los compuestos que pertenecen a esta clase no muestran actividad psicotrópica y se caracterizan por la presencia de un residuo de isoprenilo lineal no oxigenado. Aparte de los compuestos descarboxilados CBG y CBGV y sus formas parentales carboxílicas (R 2 = COOH, CBGA), todos los demás compuestos relacionados con CBGA son constituyentes menores en la producción de Cannabis . Muestran baja afinidad por CB1, aunque la prenilogación aumenta la afinidad por CB2. Además, un derivado de quinona de CBG posiblemente se une al receptor PPARγ . De hecho, como típico de CBG perteneciente a la clase β-aralquilo, amorfructina B ( 5 , Figura 1 ) se ha demostrado que es un poderoso ligando de PPARγ .
A partir de la fórmula básica de CBG, la planta convierte y produce otros cannabinoides, principalmente CBC, CBD o THC, dependiendo de las enzimas activas en el proceso. La degradación de estos compuestos ocurre espontáneamente en la planta y da como resultado CBN, entre otros. Aquí, exploramos la ruta de biosíntesis de estos cannabinoides principales.
1.2.2. Compuestos de Cannabichromene (CBC)
En este tipo de fitocannabinoide, la cadena lateral de isoprenilo se fusiona oxidativamente al anillo de resorcinol. La ocurrencia de CBC en muchas cepas de C. sativa se asocia a menudo con Δ 9 -THC, lo que sugiere una ruta biosintética común a partir del precursor común CBG. El CBC natural es racémico, muestra una fluorescencia azul bajo la luz UV y no muestra afinidad por los receptores CB1 .
1.2.3. Compuestos de Cannabidiol (CBD)
El CBD no narcótico es el principal componente fitocannabinoide en la fibra de cáñamo. La oxidasa involucrada en la formación del CBD no narcótico de CBG no está relacionada con aquellos involucrados en la formación de CBC y THC. La independencia de las rutas biosintéticas que conducen a la CDB y a delta 8 THC y Δ 9-THC, así como la observación de que los dos compuestos no se interconvierten en los tejidos de Cannabis aumenta la posibilidad de separar los efectos narcóticos de la terapéutica.
La elucidación de la configuración absoluta se realizó basándose en la correlación con el mentol natural (-). Para los compuestos de la misma clase de la serie β-aralquilo, solo unos pocos compuestos se han aislado con configuraciones absolutas y / o relativas diferentes de las aisladas del Cannabis. Machaeridiol A, B, C, utilizados como agentes antimaláricos, son representantes de esta clase .
1.2.4. Compuestos de tetrahidrocannabinol (THC)
El componente más abundante y mejor conocido de esta clase es Δ 9 -THC, junto con una gran cantidad de constituyentes menores que pueden resultar de la degradación o modificaciones de Δ 9 -THC en sí. En Δ 8 -THC, el doble enlace permanece en una posición termodinámicamente más estable y, como resultado, el proceso preferido es un desplazamiento del doble enlace de nueve a ocho posiciones . La estereoquímica integral de la estructura de Δ 9 -THC se diluyó completamente en 1964. Δ 9 -THC es menos estable que su isómero Δ 8-THC y sufre fácilmente la isomerización del doble enlace o la abstracción de la H en la posición 10a (tanto bencílico como alílico) y la eliminación a un dieno conjugado, posiblemente un precursor del CBN aromático. La forma nativa de Δ 9 -THC está representada por una mezcla de dos pre-cannabinoides carboxilados, Δ 9 -THCA y Δ 9 -THCB. El derivado carboxílico Δ 9 -THCA muestra una potente actividad neuroprotectora, que vale la pena considerar para las enfermedades neurodegenerativas y neuroinflamatorias . Δ 9 -THC actúa como un agonista parcial de CB1 y CB2 .
1.2.5. Compuestos de Cannabitriol (CBT) y Cannabelsoin (CBE)
Estos son constituyentes menores de los extractos de Cannabis, que aparecen en solo una parte de la subespecie C. sativa . CBT fue el primero en ser reconocido y aislado y solo una década después se reconoció su estructura química . CBE ( 11 , Figura 1 ) es producido por la planta en cantidades insignificantes pero también es un metabolito de CBD para los mamíferos .
1.2.6. Cannabinoids Degradant: Cannabinol (CBN) y Cannabicyclol (CBL) Compuestos
El cannabinol fue el primer fitocannabinoide caracterizado estructuralmente. El cannabinol y sus derivados ahora se consideran como el subproducto oxidativo del proceso de degradación de los compuestos de THC y CBD. El CBC se foto-degradó en CBL. Los degradantes de cannabinoides CBN y CBL muestran una baja afinidad por CB1 y CB2.
1.2.7. Cannabinoides Misceláneos
Hay otros cannabinoides no categorizados en una clase: 10-oxo-Δ-6a-tetrahidrocannabinol (OTHC); Cannabichromanon (CBCF); Cannabifuran (CBF) y deshidrocannabifuran (DCBF); Cannabiglendol; Cannabiripsol (CBR); Cannabicitran (CBT); Δ 9 -cis-tetrahidrocannabinol (cis-THC); y Tryhydroxy-Δ 9 -tetrahydrocannabinol (triOH-THC) . Sin embargo, sus cantidades relativas en la planta son bajas.
2. Discusión
2.1. Relación estructura-actividad (SAR) de los compuestos derivados del Cannabis para los receptores de cannabinoides
El objetivo principal en el estudio de la relación estructura-actividad (SAR) de los compuestos derivados del Cannabis para los receptores de cannabinoides es comprender los sitios de unión del receptor. Actualmente, solo la estructura cristalina del receptor cannabinoide humano CB1 se ha logrado completamente. Descifrar el SAR de fitocannabinoides puede ayudar a comprender mejor la farmacología y la química de los receptores de cannabinoides para desarrollar remedios dirigidos . Además, comprender los mecanismos SAR de los cannabinoides con sus receptores puede ayudar a la investigación clínica a encontrar nuevas sustancias con efectos terapéuticos y con efectos secundarios minimizados en las funciones cognitivas.
Durante los últimos 60 años, se ha llevado a cabo una considerable investigación en química médica hacia el desarrollo de SAR de los cannabinoides clásicos naturales; solo en 1986, el grupo de investigación de RK Razdan analizó el SAR de aproximadamente 300 análogos de cannabinoides según su actividad en diferentes modelos animales . Después de la identificación de Δ 9 -THC en 1964 , varias modificaciones químicas de la cadena lateral y / o el andamio tricíclico condujeron a la caracterización de familias de ligandos selectivos potentes que podrían participar en la activación del principal receptor de cannabinoides. Se ha demostrado que la cadena n -pentilo en la posición C- (3) ( Figura 1), incorporada durante la biosíntesis del ácido olivetólico , representa el grupo farmacofórico clave de THC y la modificación en esta cadena lateral conduce a cambios críticos en la afinidad, selectividad y farmacopotencia de estos ligandos relacionados con la Receptores cannabinoides ( Figura 2 ).
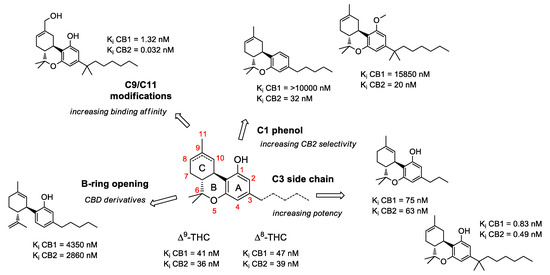
Figura 2. Ejemplos seleccionados de modificaciones químicas comunes en el esqueleto del tetrahidrocannabinol.
En general, un grupo alquilo de cadena más corta reduce la potencia del compuesto para interactuar con el receptor. En THC, por ejemplo, un grupo propilo en C- (3) crea THCV (tetrahidrocannabivarina), que muestra una reducción del 75% en la potencia a CB1 [. Un aumento en el número de átomos de carbono (hexilo, heptilo u octilo) conduce a un aumento respectivo en la afinidad y potencia para interactuar con los receptores de cannabinoides . La longitud de la cadena lateral C- (3) del THC se corresponde directamente con las afinidades de unión de CB1 y CB2, ya que un aumento en la longitud de la cadena conduce a un aumento en la afinidad de unión con los receptores de cannabinoides . Sobre la base de estas ideas, varios análogos de diferentes cadenas de carbono y anillos, con o sin incorporación de heteroátomos, pueden sugerir la predicción de un perfil SAR para una estructura dada, como el andamio de THC. Además del estudio bien establecido del objetivo candidato de la modulación de SAR basada en la cadena lateral de alquilo, se han llevado a cabo varias otras transformaciones en el núcleo tricíclico de la estructura de cannabinoides . Los compuestos cannabinoides resultantes de la reacción de apertura del anillo pirano pertenecen a los derivados de cannabidiol (CBD), que demuestran una afinidad relativamente baja a los receptores de cannabinoides CB1 / CB2 junto con una baja psico-actividad . Los primeros estudios de SAR mostraron que el anillo de pirano en la estructura cannabinoide no era un requisito para la actividad cannabinérgica en ensayos con animales. Sin embargo, varios derivados de cannabidiol con altas afinidades por los receptores CB1 y CB2 se han sintetizado e investigado a fondo . Otra posible modificación de la estructura en el andamio de THC es el grupo fenol C- (1) ( Figura 1). Los análogos de THC que carecen por completo del grupo hidroxilo fenólico, o incluso aquellos que exhiben modificaciones menores en su grupo fenólico, pueden demostrar cambios drásticos en sus capacidades farmacológicas. Se reconoció que los derivados de CBD que experimentaron la eterificación o eliminación del grupo fenol mostraron una selectividad significativa para CB2. El grupo metilo C- (11) es otro farmacóforo importante donde cambios estructurales menores pueden modular significativamente la unión del receptor ( Figura 2 ). Las sustituciones en esta posición no confieren selectividad cuando se comparan con los análogos modificados en el fenol C- (1); sin embargo, la afinidad de unión puede ser mejorada en gran medida por esta modificación.
Δ 9 -THC es un agonista para los receptores CB1 y CB2. Sus propiedades analgésicas a menudo se pasaron por alto debido a sus efectos secundarios psicotrópicos resultantes de su activación del receptor CB1. Esto ha limitado la aplicación clínica de los agonistas duales cannabinoides, a pesar de los múltiples beneficios potenciales para el tratamiento de enfermedades neurodegenerativas, entre otros . Por lo tanto, el potencial de los análogos de cannabinoides sintetizados que pueden explotar los efectos terapéuticos de los cannabinoides sin evocar las propiedades psicotrópicas no deseadas es altamente deseable y se está llevando a cabo una extensa investigación en esta dirección.
2.2. SAR de los cannabinoides y sus receptores en el tratamiento de enfermedades neuronales
Una posible perspectiva sería estudiar el mecanismo SAR de los cannabinoides sintetizados, que no evocan los efectos secundarios no deseados de los fitocannabinoides. Esto puede lograrse mediante el uso de cannabinoides que se dirijan únicamente al receptor CB2, ya que su activación no produce efectos secundarios psicotrópicos y lo convierte en el objetivo ideal para el tratamiento de varias enfermedades neurodegenerativas, incluida la enfermedad de Parkinson (EP). La EP es un trastorno crónico que implica una degradación progresiva del sistema neuronal y es la segunda enfermedad neurodegenerativa más común en todo el mundo. Actualmente no hay terapias disponibles para curar el Parkinson. Las terapias sintomáticas disponibles en la actualidad solo mejoran la calidad de vida del paciente . En el Parkinson, neuronas dopaminérgicas de la sustancia negra.(es decir, la «materia negra») del cerebro se degenera, lo que lleva a una denervación severa del cuerpo estriado que afecta la actividad motora. Este daño irreversible conduce a los síntomas motores típicos observados en pacientes con Parkinson, como bradicinesia, temblor en reposo y rigidez .
Se encontró que el líquido cefalorraquídeo de los pacientes con Parkinson sin tratar contenía altos niveles de endocannabinoides . La administración de inhibidores de la degradación de los endocannabinoides junto con un agonista del subtipo del receptor de dopamina D2 redujo los déficits motores parkinsonianos en modelos in vivo . Además, se encontró un aumento en los receptores CB1 en la lesión nigro-estriatal de pacientes con Parkinson, y en modelos de primates no humanos. Varios estudios clínicos y modelos animales sugieren que los antagonistas del receptor CB1 podrían tener valor en el tratamiento de la discinesia y los síntomas del Parkinson inducidos por levodopa, mientras que los agonistas del receptor CB1 podrían ser útiles para reducir la discinesia inducida por la levodopa. Además, recientemente se ha demostrado que un derivado de quinona de CBG tiene actividad neuroprotectora contra el daño neuronal impulsado por la inflamación en un modelo in vivo de Parkinson por la posible participación de diferentes sitios de unión en el receptor PPARγ . De hecho, se demostró en un ensayo clínico aleatorizado, doble ciego, controlado con placebo, cruzado, que la nabilona, un agonista del receptor de cannabinoides, reduce significativamente la discinesia inducida por levodopa en pacientes con Parkinson.
Sin embargo, el receptor CB2 también puede ser importante en el tratamiento del Parkinson. Se demostró que CB2 está regulado al alza en elementos gliales en tejidos postmortem de pacientes con Parkinson. Además, la activación selectiva de los receptores CB2 redujo los mediadores proinflamatorios, confirmando un modelo inflamatorio y sugiriendo que CB2 puede tener una función antiinflamatoria en esta enfermedad .
Se informó que la administración oral de extracto de C. sativa para estimular la actividad del receptor CB1 no produce mejoría en los síntomas del Parkinson , lo que sugiere que la actividad de los cannabinoides debe ser verificada, lo que puede lograrse de dos maneras. Uno sería usar una combinación de compuestos de C. sativa para mejorar la actividad. Tenga en cuenta que se sospecha que la combinación de compuestos derivados del Cannabis tiene un efecto sinérgico. Otra opción sería sintetizar análogos de cannabinoides que puedan unirse mejor a los receptores de cannabinoides, preferiblemente el CB2. De hecho, reconocemos varios esfuerzos realizados en el diseño de derivados selectivos de CB2 y en la comprensión de sus relaciones estructura-actividad y estructura-afinidad .
En este contexto, la investigación científica se centra en el desarrollo de entidades moleculares con alta afinidad por el receptor cannabinoide CB2. En los últimos años, se ha desarrollado un gran número de compuestos sintéticos selectivos de CB2 destinados al tratamiento de enfermedades neurodegenerativas en torno a una amplia variedad de andamios (hetero) aromáticos. Una encuesta bibliográfica detallada sobre el desarrollo de ligandos CB2 sintéticos se revisó ampliamente . Los derivados selectivos de CB2 se han desarrollado a partir de andamios mono- o bicíclicos que llevan heteroátomos, grupos carboxamida aromáticos o alifáticos voluminosos, y sustituyentes alquilo, arilo o arilalquilo. Los estudios centrados en la investigación de la unidad molecular responsable de la afinidad, la selectividad hacia CB2 y el perfil de actividad llevaron al diseño de un nuevo ligando de CB2 para el tratamiento y el diagnóstico temprano de las enfermedades neurodegenerativas.
2.3. SAR y perfiles de actividad de varios derivados selectivos de CB2
Se han analizado varios derivados de carboxamida (hetero) aromáticos en términos de su SAR y perfiles de actividad, incluida la oxoquinolina; naftiridinona; quinolinediona; alquiloxicumarina; indol indazol; imidazopiridina; imidazopirazina; bencimidazol; purina triazina; piridinona; bifenilo; y prolina ( figura 3 ).
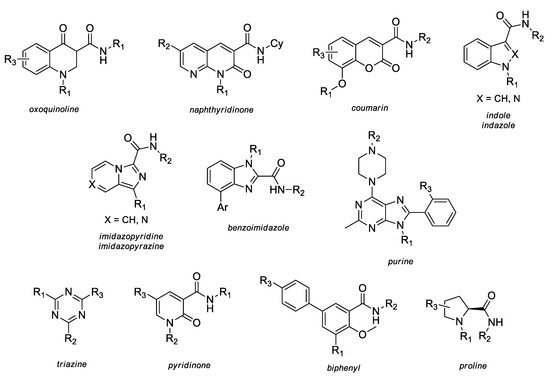
Figura 3. Los moleculas de carboxamida (hetero) aromáticos investigados en su SAR (relación estructura-actividad) y perfiles de actividad.
2.3.1. Oxoquinolina
Varios sustituyentes en la estructura de 4-oxoquinolina han sido investigados . Las afinidades altas del receptor CB pueden atribuirse principalmente a las cadenas lineales de alquilo en la posición C- (1) con el grupo n -pentilo que conduce a la afinidad relativa más alta a CB2. Los sustituyentes de cadena saturada voluminosos y lipófilos del grupo funcional 3-carboxamida conducen a altas afinidades duales. La mayor afinidad y selectividad para el receptor CB2 se logra con un anillo de adamantilo. La sustitución en la posición 6 con grupos arilo, alquilo, alquenilo o alquinilo también conduce a una alta selectividad para el subtipo de receptor CB2 .
2.3.2. Naftiridinona
Las 1,8-naftiridin-2 (1 H ) -ones muestran una alta afinidad por el receptor CB2, que está fuertemente influenciado por el sustituyente N – (1), mientras que la presencia o ausencia de un sustituyente arilo en el C- (6 ) confiere un perfil de actividad diferente .
2.3.3. Cumarina
Se ha diseñado una serie de derivados de cumarina sobre la base de un modelo de Análisis de Campo Molecular Comparativo (CoMFA) y desarrollado por Han et al. . La mejor actividad agonista de CB2R (EC 50 (CB2) = 0.144 µM, relación de selectividad CB1 / CB2 = 69.4) se encontró para los compuestos sustituidos con 8-butiloxi en R1. La incorporación de la 3-carboxamida N -atoma en un anillo de piperidina disminuyó la potencia agonista, lo que indica que la presencia de una función amida terciaria conduce a la pérdida de la actividad agonista.
2.3.4. Indol e indazol
Los estudios de SAR sobre derivados de indol revelaron que entre los medicamentos de N- indol carboxamida, los ésteres metílicos de valinato y tert-leucinato se comportan como agonistas potentes en los receptores CB1 y CB2. Recientemente, Longworth et al. estudiaron una serie de derivados de 1-alquilo y 2-alquilo indazoles, donde los isómeros 1-alquilo mostraron una alta actividad agonista de CB1 con potencias nanomolares (2.1-7.8 nM), donde la actividad de CB2 era menos potente que la actividad de CB1. Los isómeros 2-alquilo mostraron una baja potencia hacia ambos receptores cannabinoides.
2.3.5. Imidazopyridine and Imidazopyrazine
Estas dos series se probaron con respecto a los receptores de cannabinoides y su capacidad de unión a las proteínas plasmáticas. Las imidazopiridinas mostraron un perfil agonista más alto para el receptor CB2 que los derivados de imidazopirazina; además, la introducción de sustituyentes polares en R2 aumentó la capacidad de unión a proteínas plasmáticas. En general, su potencia para el receptor CB2 está modulada por modificaciones en las funcionalidades de amida (R1) y amino (R2) .
2.3.6. Bencimidazol
Se realizaron estudios de SAR en amidas de bencimidazol 2-arilmetilo o 2-alifáticas . Los compuestos que llevan R1 = etilo son más potentes y más selectivos hacia el receptor CB2 que los derivados no sustituidos en N. El derivado que tiene un sustituyente 2-clorobencilo como R2 fue el compuesto más potente hacia el receptor CB2, mostrando una selectividad de 100 veces sobre el receptor CB1. Todas las sustituciones en el arilo en R2 llevaron a una disminución general de la potencia del receptor CB2 y a la pérdida de la actividad del receptor CB1.
2.3.7. Purina
Los ligandos purínicos son potentes agonistas de CB2 y muestran una excelente selectividad hacia el receptor CB1 con buenos perfiles farmacodinámicos y farmacocinéticos y solubilidad en agua .
2.3.8. Triazina
Las 1,3,5-triazinas trisustituidas se identificaron como agonistas potentes de CB2 mediante un examen virtual basado en ligando 3D. Se desarrollaron varios antagonistas o agonistas inversos del receptor CB1 y agonistas CB2, y se identificaron los derivados más potentes de la serie en compuestos sustituidos con N– (adamantan-1-ilo) con valores de EC 50 hasta 0,60 nM .
2.3.9. Prolina
Hickey y colaboradores identificaron varios derivados de prolina mediante un enfoque de diseño de fármacos asistido por computadora (CADD) basado en una serie bien conocida de ligandos del receptor CB2 . Varios isómeros ( S ) mostraron actividades agonistas CB2 completas con altas potencias (rango picomolar) y una relación de selectividad CB2 / CB1 superior a 750, mientras que los correspondientes isómeros ( R ) mostraron un perfil agonista parcial con potencias más bajas hacia el receptor CB2. También se desarrollaron varios derivados de prolina con diferentes sustituyentes R1 y R2: los derivados de hidroxiprolina mostraron una alta potencia y selectividad de CB2, así como los derivados de ox-oxoprolina altamente solubles en agua; este último demostró alta estabilidad metabólica.
2.3.10. Piridinona
Los derivados desarrollados de 2-piridinona mostraron una alta selectividad y afinidad de CB2 cuando N-se sustituyó en la carboxamida con un anillo de cicloalquilo grande, mientras que el sustituyente en C- (5) se encontró fundamental para el perfil de actividad.
2.3.11. Bifenilo
Los estudios SAR realizados sobre carboxamidas bifenílicas mostraron una vez más que un gran anillo cicloalquilo (cicloheptilo) en la función carboxamida mejora la afinidad y la selectividad por el receptor CB2, mientras que los sustituyentes en C- (5) y C- (4 ‘) son los principales responsables de El perfil de actividad .
En resumen, oxoquinolina ( Figura 4 a), 1,8-naftiridin-2 (1 H ) -ona ( Figura 4 b), 2-piridinona ( Figura 4 c) y bifenilo ( Figura 4d) los andamios han mostrado la mayor afinidad hacia una subunidad del receptor CB2. Un análisis de las características estructurales comunes de estas clases de compuestos revela que la alta selectividad hacia el receptor CB2 requiere la presencia de un grupo carbonilo y una función carboxamida unida a un anillo de cicloalquilo. Además, la funcionalización de la posición C-1 y la presencia de un átomo de nitrógeno en el anillo cicloalquilo mejoran la afinidad, mientras que la presencia de un anillo bicíclico no es obligatoria para lograr una buena selectividad hacia CB2. Además, las modificaciones menores de las estructuras de cannabinoides tienen un efecto dramático en el comportamiento farmacológico de estos compuestos, cambiando el perfil de agonista a actividad agonista o antagonista inversa .
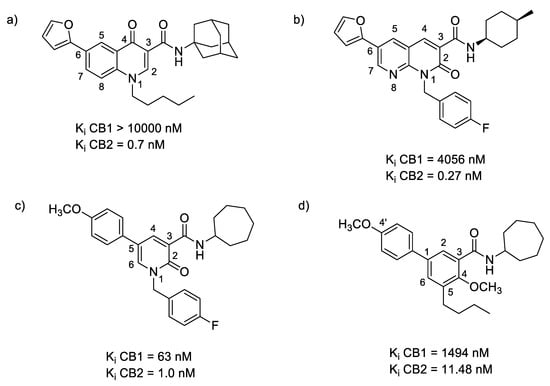
Figura 4. Los compuestos (hetero) aromáticos que muestran la mayor afinidad por los receptores CB2 en base a ( a ) oxoquinolina, ( b ) 1,8-naftiridin-2 (1 H ) -diona, ( c ) 2-piridinona y ( d) ) Estructuras de bifenilo.
3 Conclusiones
Los estudios de los mecanismos que controlan las enfermedades neurodegenerativas, junto con las observaciones sistemáticas de los tratamientos de Cannabis administrados a pacientes con enfermedades neurodegenerativas, llevaron al reconocimiento del efecto beneficioso de los cannabinoides en estas enfermedades. Sin embargo, el ensamblaje muy complicado de metabolitos secundarios en C. sativa.Los extractos, junto con la reacción psicológica no deseada que acompaña al consumo de Cannabis, llevaron a la apreciación de la importancia de la relación estructura-actividad. Los estudios de SAR son esenciales para sintetizar un cannabinoide apropiado con alta disponibilidad terapéutica y baja psicoactividad. La potencia del CBD estaba marcada, ya que tiene una psicoactividad relativamente baja debido a su baja afinidad con el receptor CB1. En este artículo, mostramos que diferentes manipulaciones menores de la estructura del CDB pueden aumentar su afinidad y capacidad de unión al CB2. También mostramos que la activación de CB2 está involucrada en afecciones neurodegenerativas, como la PD, y por lo tanto, la activación del receptor CB2 puede desarrollarse como un tratamiento para los pacientes con Parkinson. El estudio de los mecanismos de SAR entre los cannabinoides y sus receptores,Los estudios de C. sativa deben investigarse más a fondo y probarse clínicamente.
Contribuciones de autor
Conceptualización, HK y CP; Redacción-Preparación del proyecto original, HK, CP, DN y MB
Fondos
Esta investigación fue financiada por MIUR (Ministerio italiano de Universidad e Investigación) y Fondazione CRT, el cargo de procesamiento del artículo de CP fue patrocinado por MDPI.
Conflictos de interés
Los autores declaran no tener conflicto de intereses.
1Departamento de Química, Universidad de Turín, 10125 Torino, Italia
2ARO, Centro Volcani, Rishon LeZion 7505101, Israel
Autor a quien debe dirigirse la correspondencia.
Editor Académico: Antonio Evidente.
Recibido: 22 de mayo de 2018 / Aceptado: 23 de junio de 2018 / Publicado: 25 de junio de 2018
